
新冠肺炎疫情导致美国上千万人失业,经济也陷入衰退,虽然一些州开始通过逐步重启经济来缓解经济受到的重创,但如果疫苗还没有研制出来并投入广泛使用,要想在回归正常生活的同时保证人们的健康并非易事。
韩国和德国属于抗疫比较有成效的两个国家,然而在解除封锁后出现了新的感染病例。在病毒依然潜伏在人体、电梯按钮、门把手和地铁扶手上之际,美国经济实现全面重启仍困难重重。
目前研制疫苗的各种项目有100多个,能够成功的只有少数。要想预测未来几年的社会和经济会是什么样子,就必须要了解这些项目哪些能够研制成功,并且可以广泛投入使用。
因此,疫苗研制竞赛的进展和挫败不仅会影响制药板块的股价,也会影响其他板块的股价。投资者对疫苗问题的敏感程度从一个例子中可以看出来:在4月份的一个交易日里,标准普尔500指数飙升了2.7%,原因是吉利德(Gilead Sciences, GILD)宣布该公司抗病毒药物瑞德西韦(remdesivir)在一项试验中显示出对新冠病毒肺炎患者有疗效,尽管疗效很小。在接下来的一年里,股市仍会受到这类疫苗研制进展消息的影响,甚至有时可能出现非理性波动的情况。
就目前而言,投资者要想从这些项目中挑选出赢家和输家还为时尚早。目前研制还处于动物试验阶段,而且不是所有项目都有相关数据可作参考。此外,包括葛兰素史克(GlaxoSmithKline, GSK)、强生(Johnson & Johnson, JNJ)和阿斯利康(AstraZeneca, AZN)在内的许多主要制药公司已经表示,如果疫苗研制出来,它们不会在疫情期间靠疫苗来牟利。
但这场疫苗研制竞赛的确给投资者带来了一个押注未来全球疫苗业务走向的机会。疫苗可以为一些制药公司带来大量可靠的收入,赛诺菲(Sanofi, SNY)在2019年一年就销售了21亿美元的流感疫苗,葛兰素史克在2019年销售了24亿美元的带状疱疹疫苗。那些能够生产出第一批可以广泛投入使用的新冠疫苗的公司将站在全球舞台上证明自己在科研、生产和技术上的优势。
对于过去几年一直在重塑自己研发业务的辉瑞(Pfizer, PFE)这样的老牌药企来说,成功研制疫苗是证明其策略正在发挥作用的最有力的证据。对于生物技术公司Moderna (MRNA)来说,这是验证该公司一大批试验产品前景的机会,这些产品所依赖的技术和新冠疫苗所依赖的技术一样都还没有经过验证。
然而这其中蕴含的风险也不容忽视。Moderna、Novavax (NVAX)和Inovio Pharmaceuticals (INO)等规模较小的生物技术公司研制新冠疫苗的项目受到热捧,股价因此大幅上涨,但这些公司还没有上市产品。如果它们的研制项目失败,那么股价就有可能大幅回落。
目前新冠疫苗研制项目通常遵循以下两种策略之一。一些公司选用了未经验证的新技术,好处是有可能迅速取得研制进展。
如果把这场疫苗研制竞赛比作龟兔赛跑,这类公司就是比赛中的“兔子”,其中包括Moderna和辉瑞,这两家公司称最早可以在今年秋季为急救人员和高危人群提供少量疫苗。强生正在使用一种更新的技术,目标是明年初提供疫苗。
另一些公司正在使用已经经过验证的技术,但产品上市的速度会比较慢,这些公司是龟兔赛跑中的“乌龟”,主要是赛诺菲和葛兰素史克的合作项目。该合作项目使用的是赛诺菲在研制流感疫苗中使用的一种行之有效的技术,但产品要到明年夏季才能生产出来。
SVB Leerink高级分析师杰弗里·波奇斯博士(Geoffrey Porges)说,“最有可能成功的项目是那些使用已经经过验证的技术的项目,首先,事实证明这类技术是安全的;其次,这类技术已被证明对其他疾病也有效。这两点都是非常重要的保证。”
虽然使用新技术的项目可能有更多需要证明自身有效的地方,但它们也不容小觑,研制时间上九个月的差异或许意味着能够拯救几十万人的生命。
并不是所有专家都确信新冠疫苗能很快研制成功。美国每年接种的疫苗数以亿计,在受监管的几千种药品中,通过美国食品药品监督管理局(FDA)批准的不同种类的疫苗只有85种。在全世界已知的传染病中,只有25种被认为是可用疫苗预防的。获得批准的门槛很高,疫苗平均需要10年的测试,而现在我们没有那么长的时间去等待。
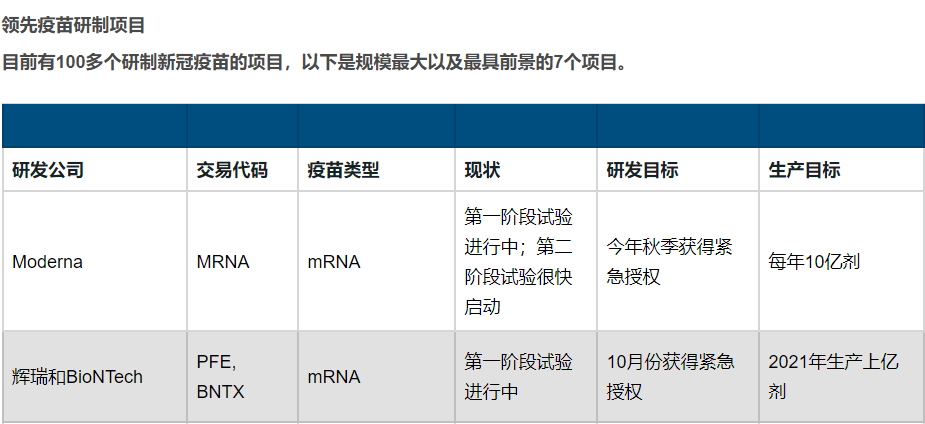
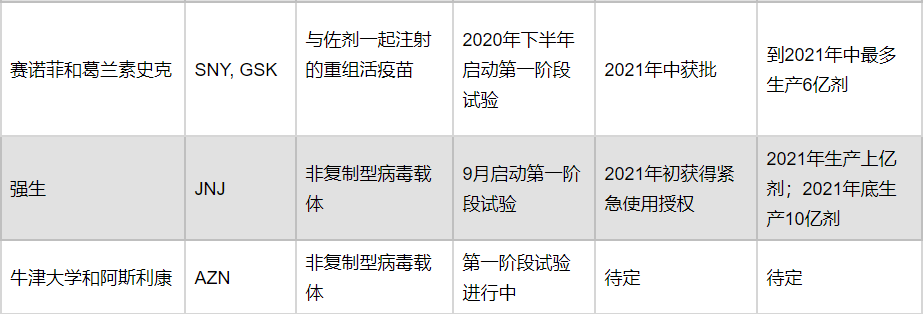

疫苗研制竞赛中的“兔子”
疫苗的工作原理是向人体的免疫系统展示一种特定病原体的安全版本,或者病原体的一部分,这样人体的自然防御系统就可以准备好抵抗真正的病原体。
研制速度最快的项目是尝试在人体内制造造成新冠肺炎的病毒SARS-CoV-2的毒株,而不是在实验室里制造。Moderna、辉瑞和其他一些公司是通过一种叫做mRNA的分子来实现这一点的,这种分子将DNA的指令带到细胞的蛋白质工厂。
强生和牛津大学(Oxford University)与阿斯利康合作的一个项目是利用一种类似于造成普通感冒的非复制型病毒实现这一点,这种病毒会将SARS-CoV-2的DNA输送到人体细胞中。
通过这两种方法,人体细胞会产生在病毒上发现的特定蛋白质,让人体免疫系统学习如何抵抗病毒。相关技术已经开发了多年,而且有些疫苗已经实现大规模生产,但FDA还没有批准任何一种通过这种方式研制的疫苗。
利用mRNA的方法似乎可以以最快的速度得出研制结果。市场对Moderna试验性疫苗的热情推动该公司股价今年暴涨220%左右。3月16日,Moderna在第一阶段安全试验中给第一个病人使用了该疫苗,并表示预计很快将开始第二阶段针对600个试验对象的试验,今年夏初将开始第三阶段试验。
Moderna预计在2021年将疫苗提交FDA审批,但该公司首席执行官斯特凡纳·班塞尔(Stéphane Bancel)表示,如果今年夏季得出的数据向好,那么该公司可能会寻求紧急使用授权,在秋季分配疫苗。
“如果能提供帮助,我们当然希望这样做,”班塞尔在4月中旬告诉《巴伦周刊》。“FDA必须做一个非常清晰的界定:即他们认为哪些人接种疫苗能够获得最好的风险回报。”
FDA可以在公共卫生危机期间发布紧急使用授权,允许使用未经批准的医疗产品。吉利德的瑞德西韦在5月份获得了该项授权。
Moderna称,该公司的目标是每年生产10亿剂疫苗,并表示能够在今年晚些时候在一个月内生产数百万剂。
辉瑞也把目标定在了今年秋季。该公司称其研制的新冠疫苗可以在10月前获得紧急使用许可或加速获得批准。辉瑞正在和德国生物技术公司BioNTech (BNTX)合作研制mRNA疫苗。在Moderna对一个候选疫苗进行测试时,辉瑞已经购买了该公司研制的mRNA疫苗的四个不同版本的使用权进行临床试验。
辉瑞首席科学官米克尔·多尔斯滕(Mikael Dolsten)说,到10月份,辉瑞将向最多8000人注射疫苗,同时还为一线工作人员或疫情严重地区的高危人群准备数百万剂疫苗供紧急使用。该公司表示将在2021年生产数亿剂疫苗。
多尔斯滕表示,辉瑞选择研制mRNA疫苗是为了在今年秋季如果暴发第二波疫情的话有所准备。他说,“我们的想法是,如果今年秋季一些地区同时暴发流感和新冠肺炎疫情的话,我们必须已经有一种能够在某种程度上投入使用的疫苗。”
多尔斯滕承认,监管机构从未批准过任何mRNA疫苗,但他说像Moderna和BioNTech这样的公司已经研究mRNA很多年了。多尔斯滕认为,这种研制方法灵活度高、速度快、可以在病毒变异时快速调整,因此比赛诺菲和葛兰素史克使用的传统方法更能有效应对疫情。
“病毒正在快速变异,我们需要使用工具和武器来对抗,”他说。“如果你的技术总是落后一步,那么就毫无帮助。”
与此同时,虽然强生的研制速度比辉瑞慢一点,但使用的技术也许是速度较快的研制项目中被证明是最有效的。这项技术使用的是一种被称为Ad26的感冒病毒的变异版,已经用于一种试验性的埃博拉疫苗,该疫苗已有5万人接种。这种疫苗还没有获得监管机构的批准,但关键的一点是,强生已经生产了200万剂这种疫苗,这是mRNA疫苗研制人员还无从获得的重要经验。
强生还开发了针对寨卡病毒、艾滋病毒和呼吸道合胞病毒的试验性Ad26疫苗。该公司表示,已经有超过6.5万人接种了这种疫苗。
“与此相关的数据库相当大,”Ragon Institute科学家丹·巴鲁克(Dan Barouch)博士说,他最先构建了Ad26病毒载体,现在正与强生合作研制新冠疫苗。与Ad26相比,其他领先的新冠疫苗研制模式缺乏大规模的临床试验经验。”
强生计划在9月前开始新冠疫苗的一期临床试验。该公司的目标是在2021年初为紧急使用授权做好准备,届时可以为卫生保健工作者和高危人群提供数千万剂量的疫苗。 强生计划到2021年第二季度生产几亿剂疫苗,到2021年年底生产超过10亿剂。
强生首席科学官保罗·斯托弗尔斯(Paul Stoffels)称,他的团队正在为第三阶段试验做准备,今年年底前试验对象达到3万到10万。斯托弗尔斯表示,由于预计病毒传播范围会很广,他并不担心与其他招募实验对象的项目之间的竞争。但如果辉瑞或Moderna的疫苗在秋季上市,那么招募工作的难度可能会加大。
这些疫苗的研制仍然可以说是一场赌博。Inovio Pharmaceuticals、牛津大学和阿斯利康合作项目以及其他一些项目也在进行中。好消息是,如果这些项目失败了,那么这场“龟兔赛跑”中的“乌龟”就不至于落得太远。
疫苗研制竞赛中的“乌龟”
赛诺菲和葛兰素史克每年总共销售近20亿剂疫苗。如果说世界上有哪家公司知道如何快速让大量人群接种疫苗,那就是这两家公司。
这两家公司的联盟是建立在赛诺菲生产Flublok流感疫苗的技术的基础上的。这项技术利用昆虫细胞来培养靶病毒表面的蛋白质,然后注射这些蛋白质来诱导体内的免疫反应。Flublok已经获得FDA批准,销售量至少达1000万剂。
赛诺菲疫苗业务子公司赛诺菲巴斯德(Sanofi Pasteur)全球疫苗研发高级副总裁约翰·希弗(John Shiver)说,“这是一项非常成熟的技术,已被证明能够成功制造疫苗。”在携手葛兰素史克之前,赛诺菲和美国政府一个名为生物医学高级研发局(Biomedical Advanced Research and Development Authority)的机构合作研制疫苗,该机构为疫苗研发提供资金。
赛诺菲首席执行官保罗·哈德森(Paul Hudson)说,“葛兰素史克知道我们的研发平台已经经过测试和验证取得成效,因为我们生产出了一种流感疫苗。葛兰素史克和我们合作是因为他们明白,虽然我们的速度会比研制mRNA疫苗慢一点,但成功概率可能更高,而且我们能够进行大批量生产。”
赛诺菲和葛兰素史克表示,两家公司将在今年下半年开始第一阶段试验,准备在明年年中提交审批申请。希弗称,届时将有1亿到6亿剂疫苗准备就绪,但这还取决于各种因素。“拥有一项以前就生产过产品的技术是一种优势,”他说。“这种生产能力是无法迅速创造出来的。”
其他公司也在研制使用类似技术的疫苗。Novavax计划在本月启动新冠疫苗第一期试验,该公司已经获得流行病防范创新联盟 (The Coalition for EpidemicPreparedness Innovations)提供的大笔资金。Novavax称其目标是在年底前获得紧急使用授权,届时可以准备好1亿剂疫苗。
无论哪家公司先把疫苗投向市场,希望它不会是最后一家。第一种疫苗可能不是最好的,许多参与这场疫苗研制竞赛的公司高管和科学家说,即使是最大的制药商也无法单枪匹马生产足够的疫苗供全世界的人接种。
巴鲁克说,“我们需要多种疫苗,因为现在还不知道哪种疫苗最安全、最有效、最耐用、最适合广泛使用。”
翻译 | 小彩
版权声明:
《巴伦周刊》(barronschina)原创文章,未经许可,不得转载。英文版见2020年5月15日报道“Inside the Science and Companies Racing to Develop a Covid-19 Vaccine”。
(本文内容仅供参考,投资建议不代表《巴伦》倾向;市场有风险,投资须谨慎。)
